

收起
活动内容收起
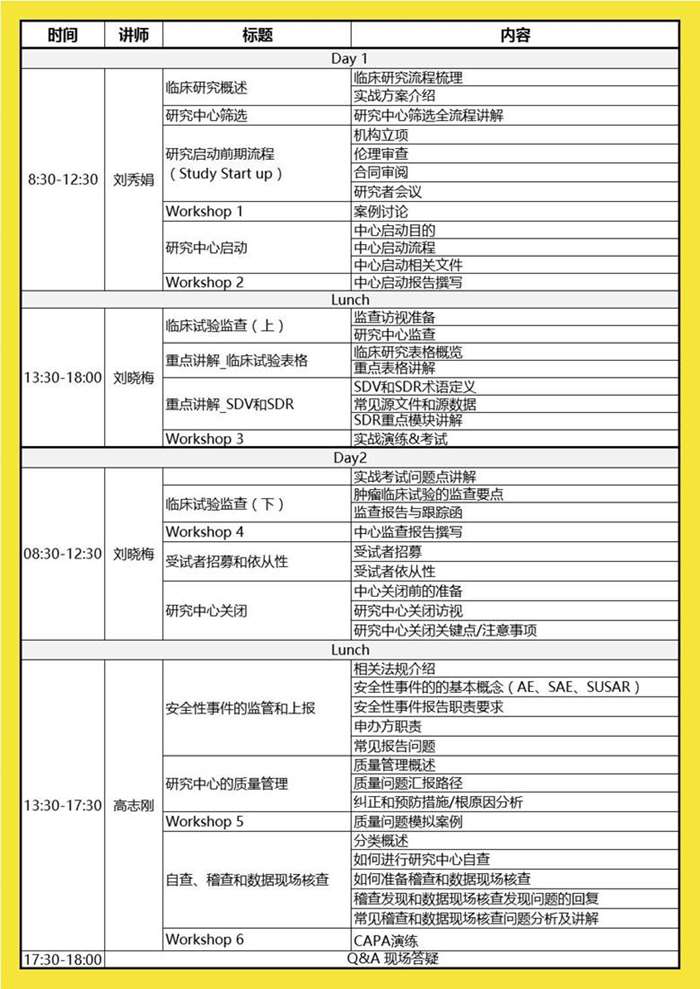
课程内容: 研究中心筛选,研究中心启动及报告撰写,监查访视及报告撰写,研究常用表格,SDV和SDR,受试者招募和依从性管理,研究中心关闭,安全性事件的管理和报告,研究中心质量管理及CAPA/Root cause 分析,稽查、核查和视察的准备和常见问题分析 课程特色: 对CRA的八大核心技能模块进行系统讲解;丰富的案例分析和随堂演练;对日常常用访视报告讲解和演练;研究相关表格和SDR重点讲解和实战演练。 课程对象: ◆ 具有一定临床试验经验希望进行系统学习或针对重点模块提高的CRA从业人员 ◆ 准备转岗CRA的CRC从业人员 所有参与者都将收到相关学习文件,包括培训日程、培训手册等。参与者在完成培训后将获得由药物临床试验网和临语堂共同颁发的结业证书。 为保证教学质量和效果,本课程将采取小班集中面对面授课,并控制参与学员人数40人以内。 课堂授课 – 讲师将就专题技能的知识和原理做出深入浅出的讲解,并针对相关内容提出问题引导参与者深入讨论。 问答讨论 – 讲师在授课过程中会就临床研究的核心流程或关键点的进行课堂提问,鼓励学员可以根据自身的经验和体会作出积极回答,以充分调动参与者的思考与反思。 案例分析分组讨论 – 按照分成的小组,就讲师提出的问题进行分组讨论,通过组内讨论和组建交流的方式,在授课讲师的引导下,结合案例分析和讨论将所学知识和技能融会贯通,掌握解决实际问题的工具和方法。 2019年11月30—12月1日(周末) 北京市 刘秀娟 某知名跨国药企QA部门总监,十余年国际多中心临床试验经验,先后就职于PPD,BMS,PRA等全球知名药厂和CRO,丰富的项目和团队管理经验,现负责公司培训平台的搭建和课程设计,以及临床部门质量体系的建立和实施等QA部门工作。 高志刚 某知名CRO公司总经理兼首席稽查官,16年临床试验行业经验,包括9年大中华区GCP,GCLP稽查经验,7年临床试验操作和管理经验,已为30余家医药研发企业和研究中心进行系统性的GCP等临床研究相关培训,同时为10余家医药研发企业建立临床试验质量管理体系。现任英国RQA会员(No.17390),长沙医学院药学系讲师,中国GCP联盟CRC行业指南编委成员,DIA 中国青年顾问团成员(YMAC),DIA-SMO协作组主任委员,北京市肿瘤协会临床试验专业委员会委员等。 刘晓梅 免疫学硕士 项目管理部门总监 12年临床研究相关经验,曾就职于泰格医药、PPD、PAREXEL和荣昌生物等国内外知名CRO和药企,项目经验涵盖肿瘤、免疫、感染、神经,心血管等多个领域I至IV期研发经验,丰富的项目管理、团队组建和人员管理经验,尤其擅长实体瘤相关研究。 现任职某知名CRO项目管理部门总监。


















 临语堂
临语堂



















